特集 : カスパーゼカスケード抗体
アポトーシスで不可欠なカスパーゼ酵素
カスパーゼファミリー酵素
すべてのカスパーゼ(アスパラギン酸特異的システインプロテアーゼ、Cysteine Aspartate-specific Proteases、Caspase)は、プロカスパーゼ(pro-caspase)と呼ばれる不活性型で合成され、活性化にはダイマー化/オリゴマー化の後、切断を受ける必要があります。
カスパーゼパスウェイポスターをダウンロード(PDF)
カスパーゼは、細胞死や炎症を含む多数のプロセスにおいて中心的な役割を果たすプロテアーゼファミリーです。アポトーシス時、一連のカスパーゼ(カスパーゼ-2、-8、-9(図1)、-10(図2)、-11、および-12)が、下流における別の一群のエフェクターカスパーゼ(カスパーゼ-3、-6 (図3)、および-7)を活性化し、これが他のタンパク質を切断してアポトーシスのプログラムが完了します。カスパーゼ-1(図4)、-4、-5、-11、および-12は、炎症に関与します。カスパーゼ-14は、アポトーシスにも炎症にも関与しませんが、皮膚細胞の発生に重要な役割を果たします。
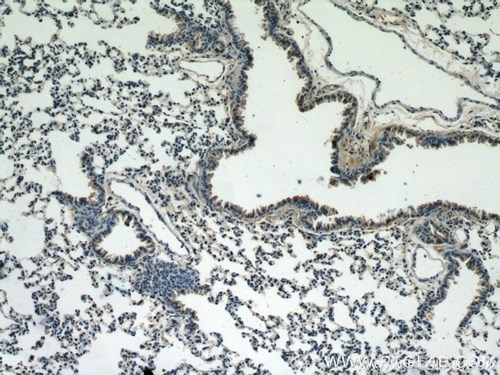 図1. 1:25の希釈倍率でカスパーゼ9/p35/p10抗体(品番:10380-1-AP)を使用したパラフィン包埋マウス肺組織スライドの免疫組織化学(10倍レンズ)。 |
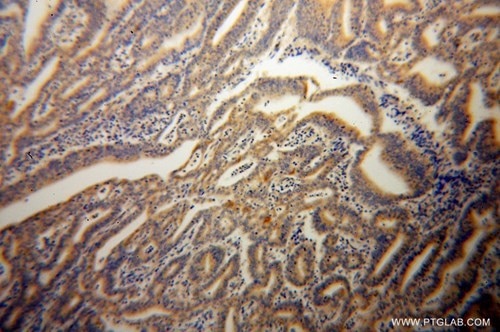 図2. 1:100の希釈倍率でCASP10抗体(品番:14311-1-AP)を使用したパラフィン包埋ヒト子宮内膜癌の免疫組織化学(10倍レンズ)。 |
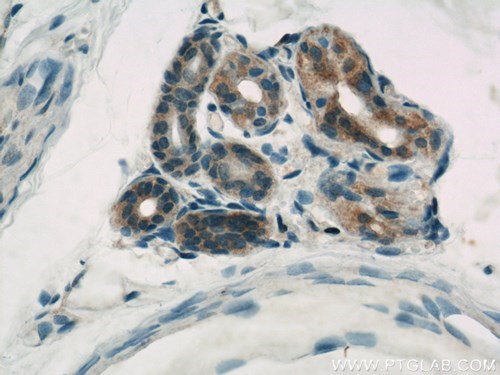 図3. 1:500の希釈倍率でCASP6抗体(品番:10198-1-AP)を使用したパラフィン包埋ヒト皮膚の免疫組織化学(40倍レンズ)。 |
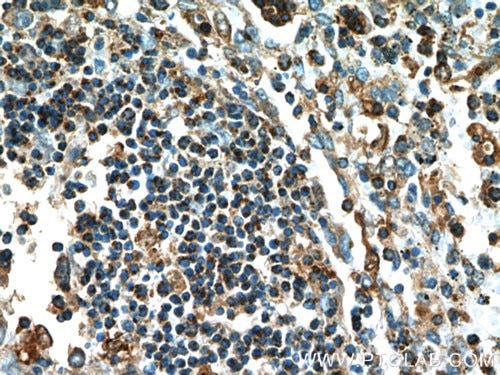 図4. 1:200の希釈倍率でカスパーゼ1抗体(品番:22915-1-AP)を使用したパラフィン包埋ヒト脾臓組織スライドの免疫組織化学(10倍レンズ)。 |
2種類のカスパーゼ経路
アポトーシス促進タンパク質(Pro-apoptotic protein)と抗アポトーシスタンパク質(anti-apoptotic protein)は、おそらくアポトーシス刺激後の最初のカスパーゼ標的です。外因性または内因性の細胞死シグナルは、2種類の明確に異なる経路を介してカスパーゼを活性化、アポトーシスを媒介します。外因性経路は、細胞表面の細胞死受容体にリガンドが結合することによって始動し、内因性経路は、DNA損傷、増殖因子の減少、細胞外マトリックスとの接着の喪失などの要因によって活性化され、ミトコンドリアによって媒介されます。
アポトーシスにおけるカスパーゼ-3とカスパーゼ-8
カスパーゼ-3および-8は、アポトーシス反応の重要な調節因子です。カスパーゼ-8(図5)はアポトーシスの開始に重要です。活性型カスパーゼ-8はカスパーゼ-3を切断し、その結果細胞死が誘発されます。カスパーゼ-3(図6)は、アポトーシスの重要なメディエーターの1つとして同定されました。Bcl-2とBcl-XLを切断して、これらのタンパク質の抗アポトーシス機能を失わせると共に、アポトーシスを促進するC末端断片を遊離させます。アポトーシス活性化に後天的欠陥があると、多くの場合、細胞増殖の制御不良、発癌、および癌につながります。腫瘍壊死因子(TNF)受容体にリガンドが結合すると、FADDや他のデスドメインアダプタータンパク質が動員され、それらがカスパーゼを動員・活性化することによってアポトーシスが開始されます。
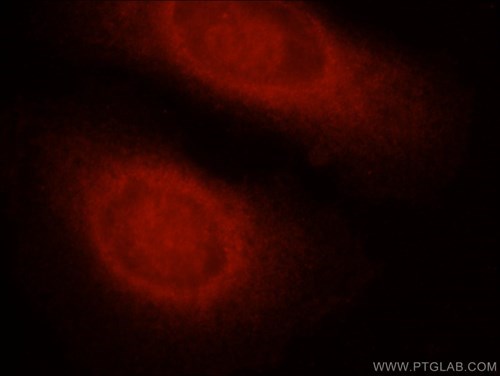 図5. 1:25の希釈倍率でカスパーゼ8抗体(品番:13423-1-AP)をローダミン-ヤギ抗ウサギIgGと共に使用したHepG2細胞の免疫蛍光分析。 |
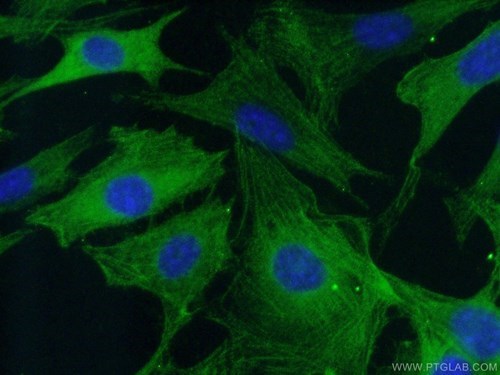 図6. 1:50の希釈倍率でカスパーゼ3抗体(品番:19677-1-AP)をAlexa Fluor 488コンジュゲートAffiniPureヤギ抗ウサギIgG(H+L)とともに使用した(-20°Cエタノール)固定NIH/3T3細胞の免疫蛍光分析。 |
