サイトカイン&増殖因子
ヒト細胞(HEK293細胞)発現系で産生したサイトカインおよび増殖因子は、優れた生物学的活性と安定性、ロット間一貫性、グリコシル化を含む「ヒト型」の高レベルの翻訳後修飾、コンフォメーション(フォールディングや成熟)を実現します。
プロテインテックのヒト発現系は、ヒトネイティブ型のコンフォメーションを取り、ヒト型の翻訳後修飾を受けた優れた生物活性を示す組換えタンパク質を産生します。タグフリーの組換えタンパク質は、アニマルフリーおよびゼノフリー条件下で産生され、エンドトキシンフリー製品としてキャリアフリー包装にて提供されます。
アニマルフリー
エンドトキシンフリー
ゼノフリー
タグフリー
キャリアフリー
HumanKine®(ヒューマンカイン)組換えタンパク質は、アニマルフリー条件下でヒト細胞(HEK293細胞)から産生されます。
大腸菌等の細菌発現系により得られるタンパク質は、リン酸化やグリコシル化等の翻訳後修飾を受けていません。 多くのタンパク質は、その生物学的活性を発揮するために、真核生物の発現系でのみ施される糖鎖修飾やプロセシングを必要とします。つまり「本物」のヒトタンパク質にはヒト細胞発現系が必要となります。
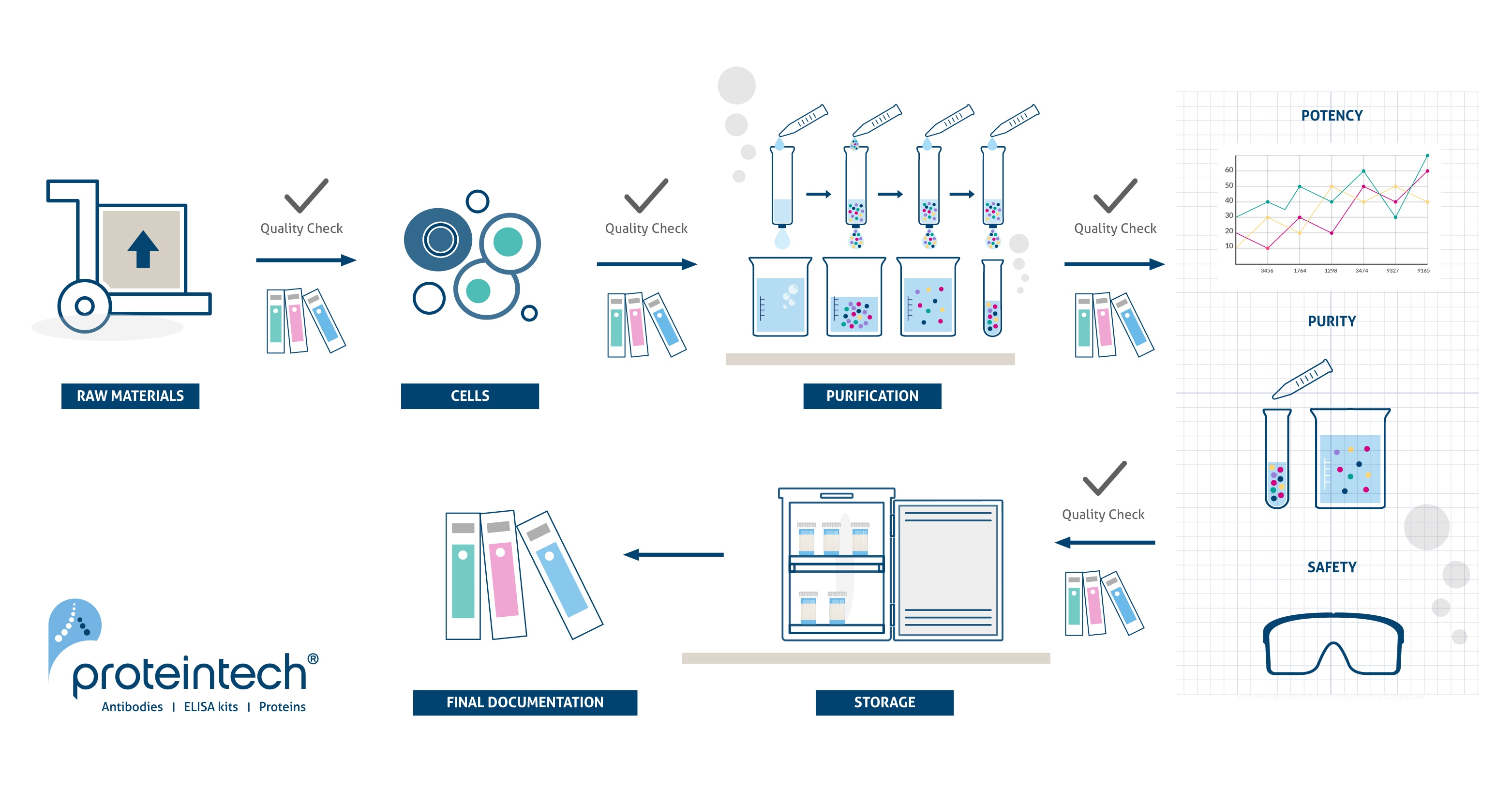
すべての『HumanKine® 組換えタンパク質』製品は、自社のcGMPグレードラボで厳格な品質管理規定に従って製造されます。
-
「本物」のヒトタンパク質
-
ヒトネイティブ型のコンフォメーション&翻訳後修飾
-
優れた生物学的活性&安定性
-
標準研究グレードからcGMPグレードに「シームレス」な移行が可能
標準研究グレード vs cGMPグレード
非臨床試験/非臨床研究から臨床試験/臨床研究へスムーズに移行するために、HumanKine®(ヒューマンカイン)は様々な 標準研究グレードの組換えタンパク質 およびcGMPグレードの組換えタンパク質を提供しています。 標準研究グレードおよびcGMPグレード製品は、いずれもcGMPグレード施設において同一の発現系、製造工程、作業手順によって製造されています。 したがって、2つのグレード間における品質面および性能面の違いは実質的にはありません。
プロテインテックの標準研究グレード製品とcGMPグレード製品の大きな違いは、ISO 13484認証およびcGMP準拠の厳格な品質プロセスに準拠しているかどうかです。 cGMPグレード製品の場合、規制に沿った文書化、徹底したQC、トレーサビリティ対応を実施しています。 標準研究グレード製品は、信頼性の高い製品として、初期の研究開発段階で高い費用対効果を提供します。
cGMP製造プロセス
Frequently Asked Questions
What is the stability of HumanKine proteins?
Unless specified otherwise in the product information sheet, our products are formulated to ensure the stability of lyophilized proteins at room temperature. It is advised to store lyophilized products at -20°C to -80°C. For reconstituted solutions of most products, short-term storage at 4°C is recommended. Extended storage of the protein solution should be at -20°C to -80°C. Keep in mind that each freeze/thaw cycle may lead to some protein denaturation, so it is not recommended to subject aliquots to multiple freeze/thaw cycle.
Why are some proteins reconstituted in acidic buffer?
Acid reconstitution buffer is especially important for proteins with a high isoelectric point, making the molecule hydrophobic at neutral pH. Failure to use the recommended buffer may result in incomplete dissolution of the cytokine or its potential loss on the surfaces of labware such as pipet tips, vials, and test tubes. Diluting the protein aliquots to the working concentration in the appropriate buffer for a specific application helps neutralize the small amount of acid added, ensuring the safe use of the protein with live cells.
Is it ok to replace Human Serum Albumin (HSA) with Bovine Serum Albumin (BSA) in reconstitution buffer?
Bovine serum albumin (BSA) can be used instead of Human Serum Albumin (HSA) in reconstitution buffer. We recommend to use recombinant HSA to keep the product animal component free. If your experiment will not be impacted by the presence of animal derived components, BSA containing buffer can be used for reconstitution.
Can HumanKine cytokines cross-react with mouse cells?
Except for a few cases, the majority of human cytokines exhibit activity on mouse cells. While many mouse cytokines can act on human cells, their specific activity might be lower compared to the corresponding human cytokine. Species specificity is observed in certain cytokines, such as interferons, GM-CSF, IL-3, and IL-4, which have minimal to no activity on non-homologous cells. In contrast, FGFs and neurotrophins are highly conserved, displaying robust activity on cells from various animal species.
How is HumanKine protein bioactivity calculated in international units(IU)?
International Unit (IU) values for our Humankine products are obtained by conducting multiple side-by-side comparisons with the WHO Reference Standard within our biological activity assay. This approach involves performing several comparison tests to account for potential outliers arising from variations in the assay, such as differences in the product, handling, assay protocol, and more. To learn more about international unit calculation, read our blog.
Why does my lyophilised protein vial appear to be empty?
The lyophilized product may have shifted from the vial's bottom during shipping/handling, scattering on the vial wall or cap. A firm tap on the bench or a brief spin in a centrifuge can help reposition the lyophilized product back to the vial's bottom. Certain pellets may present themselves as a minimal amount of material or a transparent film, attributed to the characteristics of the original buffer formulation. This appearance is typical for numerous proteins and is considered normal.
関連資料
樹状細胞を分化誘導する時間を短縮—HumanKine® GM-CSFとIL-4を使用すれば培地交換不要(英文)
HumanKine® IL-23でヒトTh17細胞の誘導効率を100倍以上に(英文)
ヒト細胞発現組換えタンパク質 HumanKine® TGF-β1、TGF-β2、TGF-β3によるヒトTh17細胞の効率的な分極化について(英文)
HumanKine® TGF-β1による効率的なTh17細胞の誘導(英文)
組換えヒトタンパク質の生物学的機能および活性におけるネイティブ型糖鎖修飾の重要性(英文)
自己免疫疾患研究に有用なツール—HumanKine® IL-17(英文)
効率的なTh17細胞分化に—ヒト細胞発現組換えタンパク質 HumanKine® サイトカイン(英文)
HumanKine® Noggin—ヒト細胞発現による糖鎖修飾ジスルフィド結合型二量体(英文)
論文使用実績
Front. Bioeng. Biotechnol.
Mechano-Hypoxia Conditioning of Engineered Human Meniscus
Alexander R A Szojka
Br J Pharmacol
Yanhong Pan
Int Immunopharmacol
Siqi Shao
Proc Natl Acad Sci U S A
Takahiro Nishio
Nat Commun
Extracellular mRNA transported to the nucleus exerts translation-independent function
Takeshi Tomita
特集/ブログ記事
Top 4 considerations when choosing your recombinant proteins
Due to the importance in cell culture and therapeutic systems, there are several considerations to evaluate when choosing a recombinant protein for your own cultures.
6 reasons why HEK293 proteins are superior for clinical applications
Find out the benefits of HumanKine® recombinant proteins, cytokines and growth factors.
Top 4 considerations when choosing your recombinant proteins
Due to the importance in cell culture and therapeutic systems, there are several considerations to evaluate when choosing a recombinant protein for your own cultures.
6 reasons why HEK293 proteins are superior for clinical applications
Find out the benefits of HumanKine® recombinant proteins, cytokines and growth factors.
FGF Basic TS
Thermostable FGF does not require media changes over the weekend.