抗がん治療に革命をもたらす免疫チェックポイント阻害剤
Sepideh Jahangiri著(Montreal大学、Ph.D. Candidate)
19世紀後半に、William B. Coleyは現代的な免疫療法の基礎を築きました。整形外科医として勤務していた頃に、Coleyは術後感染症を発症したがん患者の腫瘍が自然退縮する症例を何例か観察し、他にも同様の事例が報告されていることを知りました。Coleyは、感染を契機に活性化した免疫系が、がんと闘ううえで何らかの役割を果たしているのではないかという仮説を立てました。1891年にColeyは仮説の検証を開始し、免疫反応を誘発するために、Streptococcus pyogenes(化膿レンサ球菌)やSerratia marcescens(セラチア菌)等の生菌や不活性化した菌、それらの混合物をがん患者に注射する治療を試みました。「Coley's toxin(コーリートキシン)」として知られる菌毒素の調合物によって、ある種のがんでは著明に寛解する例も認められましたが、明確な作用機構は不明で感染リスクも伴うことから、医学界からは懐疑的に受け止められました(1)。
Coleyの試みの背景にある免疫学的原理を研究者が解明したのは、それから数十年後のことでした。当時、がんに対する免疫系の役割については懐疑的な見方が優勢でした。例えば、British Journal of Cancer誌に掲載され数多く引用されている論文では、マウスにおいて自然発生した27種類の腫瘍に免疫原性は認められなかったことから、移植腫瘍モデルを用いた報告で観察される免疫反応はウイルスや化学物質によって誘導されたアーチファクトである可能性が高いと結論付けられました(2)。がんと免疫系が関与する治療法の問題点について述べた別の論評では、「as difficult to reject the right ear and leave the left ear intact as it is to immunize against cancer(正常組織を傷つけず、がんだけに免疫を誘導するのは難しい)」(3)と、その実現性は疑問視されていました。顕著な毒性と予測不可能な反応により初期段階の試みは挫折したものの、一連の取り組みによって現在のように洗練された免疫系を基盤にした有効性の高い抗がん治療への道が拓かれました。
2013年にScience誌は、他の進歩的な成果を凌駕し、腫瘍学における重要な契機をもたらしたとして、がん免疫療法を「Breakthrough of the Year」に選出しました。がん免疫療法は臨床試験を通じて切除不能な進行性がんや転移がんに対して有効性を示し、患者の生存期間を有意に延長することを証明した点がこのような高い評価に繋がりました。免疫療法の発展は、CRI(Cancer Research Institute)Scientific Advisory Councilの責任者であるJames Allison博士と、CCII(Center for Cancer Immunotherapy and Immunobiology)所長の本庶佑博士による画期的な業績によって活発化しました。彼らは、免疫チェックポイントに関わる受容体であるPD-1(Programmed cell death 1)とそのリガンドであるPD-L1や、CTLA-4(Cytotoxic T lymphocyte-associated protein 4)といったタンパク質に関する研究で、2018年のノーベル生理学・医学賞を受賞しました(4)。
|
|
免疫編集:がんと免疫系の終わらない攻防
免疫学的な観点からみると、免疫編集(Immunoediting)という概念は、がんが免疫系に対抗してどのように進化するか、その機構について解き明かしています。免疫系は異常な細胞を認識・排除すると同時に正常な組織に対する寛容性を維持して、常に繊細な均衡を保っています。この免疫編集は、排除(elimination)・均衡(equilibrium)・逃避(escape)の3段階の過程(相)で構成されます。
- 排除の過程では、がん細胞が臨床的に顕著な腫瘍を形成するよりも前に、免疫系ががん細胞を検知し排除する機構が働きます。細胞傷害性T細胞、ナチュラルキラー(NK)細胞、マクロファージなどの免疫細胞が、腫瘍抗原や細胞の異常を認識して悪性細胞を排除します。
- 均衡の過程では、免疫系に発見されにくく変異した一部のがん細胞が生存する状態にあります。この過程では、がんは制御された状態にあるものの、完全には根絶されていません。
- 逃避の過程では、がん細胞はMHCクラスI分子の下方制御によって腫瘍抗原が検出されにくい状態になるか、あるいは免疫抑制性の腫瘍微小環境(TME:Tumor microenvironment)を形成して免疫系に認識されにくくなり、免疫系による攻撃を回避します。腫瘍微小環境下では、PD-L1等の分子ががん細胞に、PD-1やCTLA-4等の分子が免疫系細胞に多く発現し、免疫細胞の活性化が阻害され、腫瘍増殖が促進されます。
|
プロテインテックの関連製品 |
||
免疫療法の中でも免疫チェックポイント阻害剤(ICI:Immune checkpoint inhibitor)は、この免疫回避(Immune escape)状態の打破を試みる医薬品です。免疫チェックポイント阻害剤は免疫系の活性化を抑える分子(例:PD-1、CTLA-4)をターゲットとすることで、腫瘍微小環境という抑制性の条件下であっても免疫細胞の作用を増強し、腫瘍細胞を認識・攻撃するよう働きかけます(5)。
免疫チェックポイント分子PD-1とCTLA-4の作用機序
免疫系は、病原体への攻撃と、自己免疫を防ぐための寛容性の維持との間の微妙な均衡を正確に保たなければなりません。PD-1とCTLA-4は、この均衡の制御に働きかける共抑制受容体の中でも最も重要な受容体です。この2種類の受容体はどちらもT細胞活性化を抑制する働きを示しますが、その作用機序や発現部位は異なります。
- CTLA-4は、主にリンパ組織におけるT細胞活性化の初期段階で作用します。ナイーブT細胞が抗原提示細胞に接触すると、T細胞の活性化に伴って誘導されるCTLA-4は共刺激受容体CD28と競合的に、抗原提示細胞が表出するB7分子に結合します。T細胞活性化シグナルを伝えるCD28と競合することで、CTLA-4はT細胞活性化の最初の段階を抑制し、過剰な免疫活性化を回避する働きを示します(6)。
- PD-1は、CTLA-4とは別に、主に免疫細胞がエフェクター機能を発揮する末梢組織において、免疫応答の後期段階で作用します。PD-1は活性化T細胞、B細胞、骨髄系細胞上に発現し、そのリガンド(PD-L1・PD-L2)と結合すると、抑制性のシグナルがT細胞に伝達されてT細胞活性が減弱します。この機序は、免疫系の恒常性を維持する働きを示し、健常組織における自己免疫反応を防ぐうえで極めて重要です(7)。
免疫チェックポイント阻害剤は、こうしたチェックポイント分子を阻害する働きによって、T細胞の抑制を解除して腫瘍殺傷機能を増強します。PD-1やCTLA-4によるシグナル伝達経路を阻害すると免疫反応が長期にわたり持続し、免疫回避のために腫瘍が利用する防御機構を免疫系が克服し、腫瘍に対して抗腫瘍効果を発揮できるようになります。その結果、従来であれば治療困難、あるいは治療できないとみなされていた腫瘍を中心に、様々ながんにおいてこれまでにない治療効果が得られています。
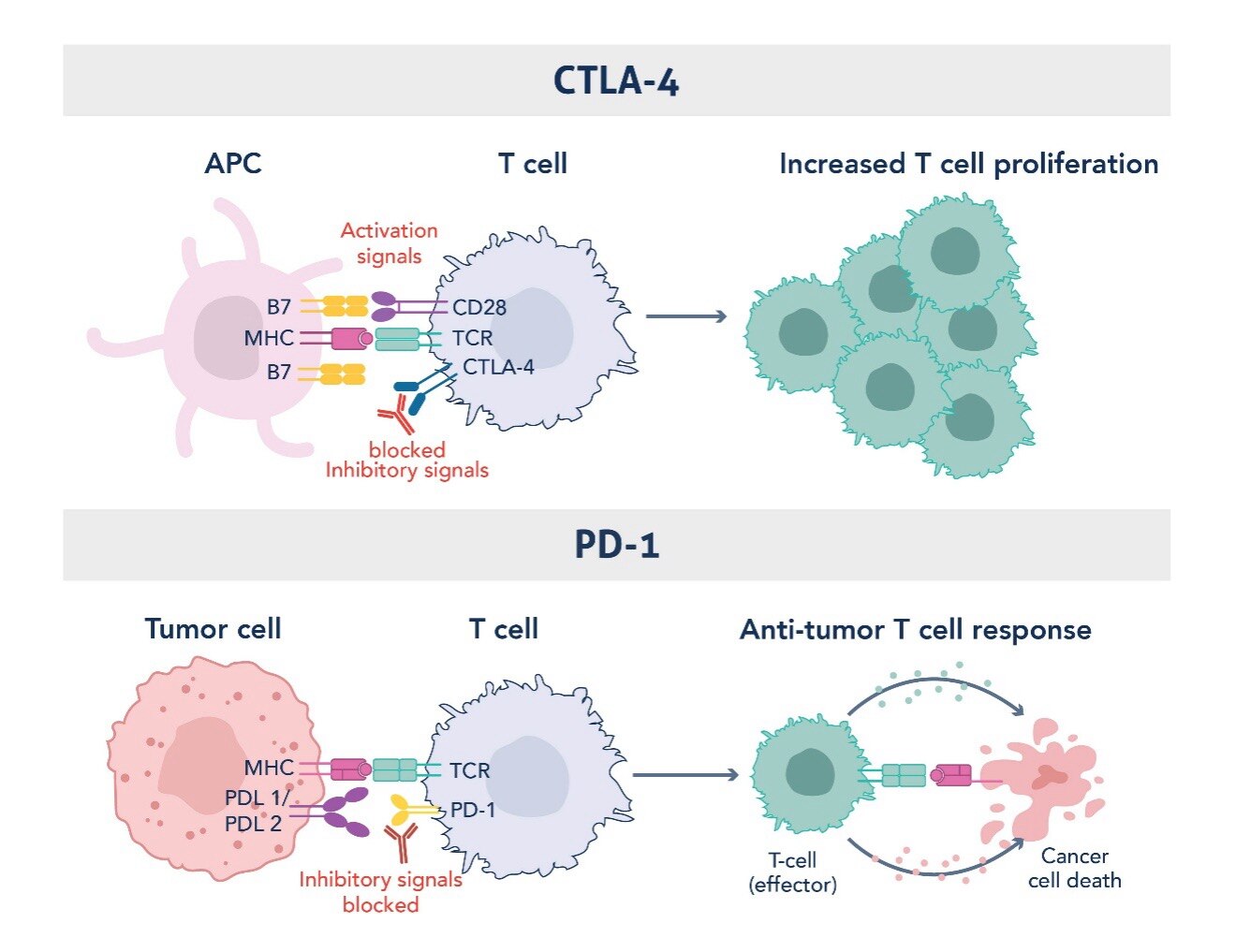
図1. CTLA-4・PD-1免疫チェックポイント分子と過剰なT細胞の活性化や機能の抑制に関与する因子。本図はSharma et al. 2023(PMID: 37059068)(8)に掲載された図を編集しています。
画期的な新薬と有望な将来性
CTLA-4阻害剤であるイピリムマブ(Ipilimumab、販売名:ヤーボイ)は、根治切除不能な悪性黒色腫に対する治療薬として、2011年にFDAに初めて承認されました。その後、2014年に抗PD-1抗体であるニボルマブ(Nivolumab、販売名:オプジーボ)が切除不能又は転移性の悪性黒色腫に対する治療薬として日本で販売承認され、同じ免疫チェックポイント阻害剤であるイピリムマブとの併用療法の臨床試験が実施されるなど(9)、他の抗悪性腫瘍剤との併用が効果を示すことが認められ、その適応が拡大しています。また、同じ2014年には、抗PD-1抗体であるペムブロリズマブ(Pembrolizumab、販売名:キイトルーダ)がイピリムマブや他の医薬品による治療後に疾患進行が認められた切除不能又は転移性の悪性黒色腫に対する治療薬としてFDAに迅速承認されました。ペムブロリズマブは、非小細胞肺癌(NSCLC)、手術不能又は再発性のPD-L1陽性トリプルネガティブ乳癌、根治切除不能な尿路上皮癌、子宮頸癌等の治療薬として用いられ、多種に及ぶ悪性腫瘍の第一選択薬となっています。
LAG-3、TIGIT、VISTA、B7-H3、IDO、TIM-3、CD47、CD39、CD73、CD40、OX40、GITRといった分子は、奏効率を高め薬剤耐性を克服する手掛かりとなる可能性を秘めており、研究者は新たな免疫チェックポイント経路の探索を進めています。こうした研究の隆盛は免疫チェックポイント阻害剤による治療の適応の拡大を狙い、重複しない新規経路をターゲットとすることで、様々ながんに対する有効性を向上させることを目的としています。さらに、化学療法、放射線療法、腫瘍選択性を高めた治療法(集束超音波治療、光線力学的療法、ナノ粒子送達技術、腫瘍溶解性ウイルス療法に加え、様々な治療法が考案されています)といった別の治療法と免疫チェックポイント阻害剤を併用することで、有効性の向上を図り、治療抵抗性を克服し、副作用を最小限に抑える抗がん治療が模索されています。このような戦略は、幅広いがんに対して長期奏効し良好な転帰を示すがん治療を提供することを狙いとしています。
|
プロテインテックの関連製品 |
||||
| GITR |
|
|
||
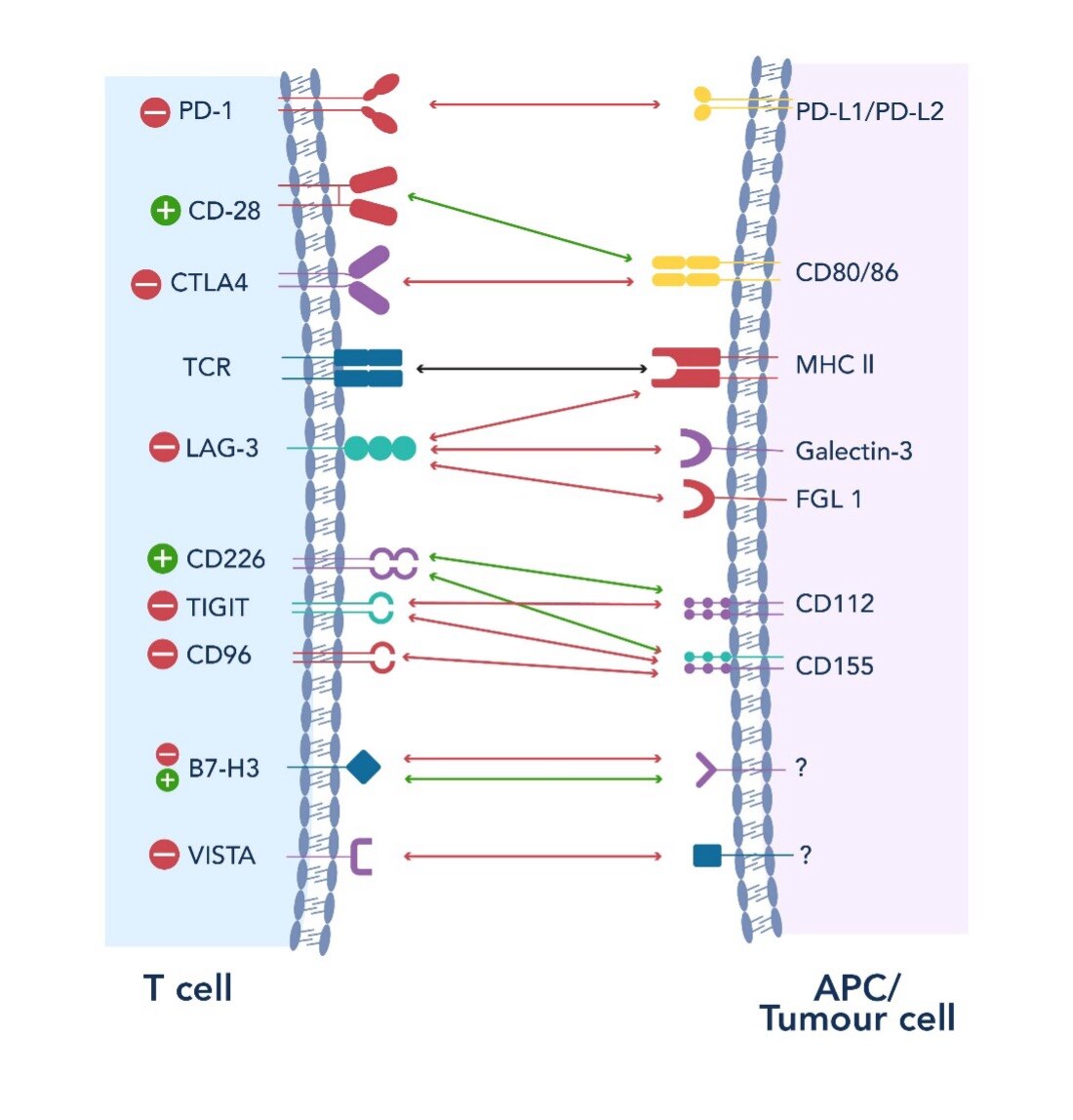
図2. がんの進行と治療における新規免疫チェックポイント経路の全体像
個別化免疫療法の今後の方向性
免疫チェックポイント阻害剤による抗がん治療の領域における個別化免疫療法は今後、大きく進展すると考えられます。この分野の発展に伴い、免疫チェックポイント分子の作用機序のさらなる解明と、多岐にわたるチェックポイント分子を標的とする新規併用療法の確立が強く求められています。二重特異性抗体や抗体薬物複合体のような抗腫瘍効果の増強を狙う革新的な次世代型の抗体についても、現在研究が進められています。ネオアンチゲン(新生抗原)ワクチン、腫瘍浸潤リンパ球(TIL:Tumor-infiltrating lymphocyte)輸注療法、バイオマーカー主導型治療等の個別化医療は、治療効果を最適化すると同時に副作用を最小限に抑えられるようデザインされています。さらに、患者個人に特化したマルチオミクス解析や包括的な免疫プロファイリングは、治療開始に先立った腫瘍の特徴の識別に有望で、それぞれの患者にあわせた治療計画の策定を可能にします。注目すべき点として、ネオアジュバント療法に免疫チェックポイント阻害剤を適用した結果、顕著な腫瘍退縮と良好な免疫応答が認められています。この研究の有用性は、局所進行dMMR(ミスマッチ修復機構欠損)結腸・直腸癌患者において高いMPR(Major pathological response)率を示した報告によって裏付けられています(10、11)。このような研究は、免疫チェックポイント阻害剤が従来の化学療法の代替となる可能性を明示するだけでなく、一連の研究で明らかになった知見を検証するために、追跡期間を延長し、規模を拡大した研究を実施する必要性を強調しています。免疫チェックポイント阻害剤を使用した抗がん治療について現行の研究や将来的な臨床応用を最適化するには、がん免疫療法を実施する適切な開始時期、併用する治療法の種類、投与順序、投与方法等を評価し、適切な適格基準を確立することが極めて重要となります(12)。有効性や有害事象の予測には、正確性の高いバイオマーカーを特定する必要がありますが(13)、それと同時に有害事象の迅速な診断と管理を重視しなければなりません。免疫チェックポイントの機序解明や治療ガイドラインの整備、将来的には、より効果が高く個別化されたがん免疫療法を実現するために、今後も前臨床研究や臨床研究を積み重ねる必要があります。
参考文献
- E A Carswell et al. An endotoxin-induced serum factor that causes necrosis of tumors. Proc Natl Acad Sci USA. 1975 Sep;72(9):3666-70.
- H B Hewitt, E R Blake, A S Walder. A critique of the evidence for active host defence against cancer, based on personal studies of 27 murine tumours of spontaneous origin. Br J Cancer. 1976 Mar;33(3):241-59.
- W H Woglom. Immunity to Transplantable Tumours. Cancer Review. 1929 May 22;4:129-214.
- J Couzin-Frankel. Breakthrough of the year 2013. Cancer immunotherapy. Science. 2013 Dec 20;342(6165):1432-3.
- M M Gubin, M D Vesely. Cancer Immunoediting in the Era of Immuno-oncology. Clin Cancer Res. 2022 Sep 15;28(18):3917-3928.
- S C Wei, C R Duffy, J P Allison. Fundamental Mechanisms of Immune Checkpoint Blockade Therapy. Cancer Discov. 2018 Sep;8(9):1069-1086.
- A H Sharpe, K E Pauken. The diverse functions of the PD1 inhibitory pathway. Nat Rev Immunol. 2018 Mar;18(3):153-167.
- P Sharma, S Goswami, et al. Immune checkpoint therapy-current perspectives and future directions. Cell. 2023 Apr 13;186(8):1652-1669.
- J D Wolchok, et al. Nivolumab plus ipilimumab in advanced melanoma. N Engl J Med. 2013 Jul 11;369(2):122-33.
- M Chalabi, Y L Verschoor, et al. Neoadjuvant Immunotherapy in Locally Advanced Mismatch Repair-Deficient Colon Cancer. N Engl J Med. 2024 Jun 6;390(21):1949-1958.
- A Cercek, et al. PD-1 Blockade in Mismatch Repair-Deficient, Locally Advanced Rectal Cancer. N Engl J Med. 2022 Jun 23;386(25):2363-2376.
- M Kwon, I-S Kim, et al. The right Timing, right combination, right sequence, and right delivery for Cancer immunotherapy. J Control Release. 2021 Mar 10;331:321-334.
- J J Havel, D Chowell, T A Chan. The evolving landscape of biomarkers for checkpoint inhibitor immunotherapy. Nat Rev Cancer. 2019 Mar;19(3):133-150.
